目前,在中国上市的相关儿童用多联疫苗只有一种四联疫苗和一种五联疫苗。这两种多联疫苗均为独家品种,无细胞百白破b型流感嗜血杆菌联合疫苗(四联苗)由康泰生物子公司北京民海生物科技生产,吸附无细胞百白破灭活脊髓灰质炎和b型流感嗜血杆菌(结合)联合疫苗(五联苗)由赛诺菲巴斯德生产。
中国国内已上市相关多联疫苗
| 四联疫苗 | 五联疫苗 | |
| 疫苗简称 | DTaP-Hib | DTaP-IPV-Hib |
| 生产厂商 | 北京民海生物科技(康泰生物子公司) | 赛诺菲巴斯德 |
| 免疫程序 | 3/4/5/18月龄 | 2/3/4/18月龄 |
| 共4剂次 | 共4剂次 | |
| 接种年龄 | 3月龄以上 | 2月龄以上 |
| 用量规格 | 0.5ml | 0.5ml |
数据来源:NMPA,民海生物科技、赛诺菲官网
儿童用四联、五联疫苗获批签发数据
受新冠疫情及新冠疫苗集中接种影响,2021年后,我国疫苗批签发批次数据整体有所下降。四联苗批签发2020年与2021年同比减少18%,2021年与2022年同比减少26%,四联苗批签发在2022年后有所恢复,2021年第四季度(9批次)与2022年第四季度(16批次)同比增加78%。
五联苗2020年与2021年同比下降15%,2021年与2022年同比增长27%,2021年第四季度五联苗获批签发21次,2022年第四季度五联苗获批签发12次,同比下降43%。
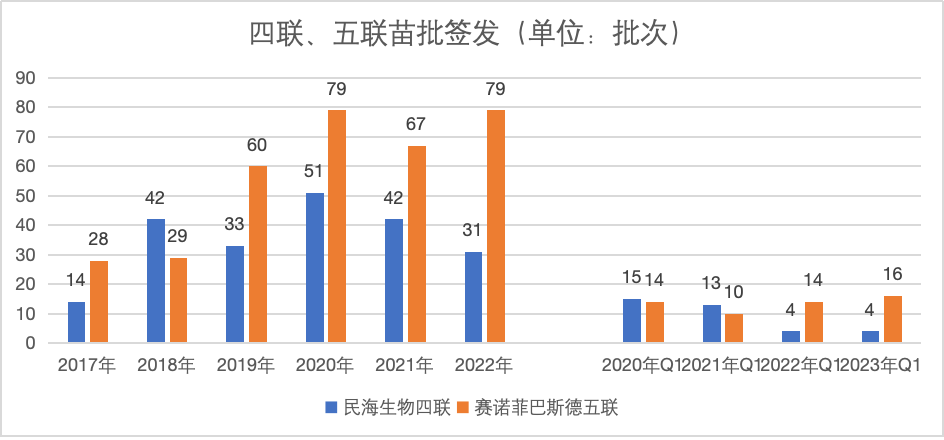
2022 年,康泰生物子公司北京民海生物科技生产的四联疫苗全年批签发为 31 批次(-26.19%), 赛诺菲巴斯德生产的五联苗批签发 79 批次(+17.91%)。2023年第一季度,民海生物的四联苗批签发 44万支,与上年同期持平;赛诺菲巴斯德的五联苗批签发128万支,较上年同期增长14.29%。
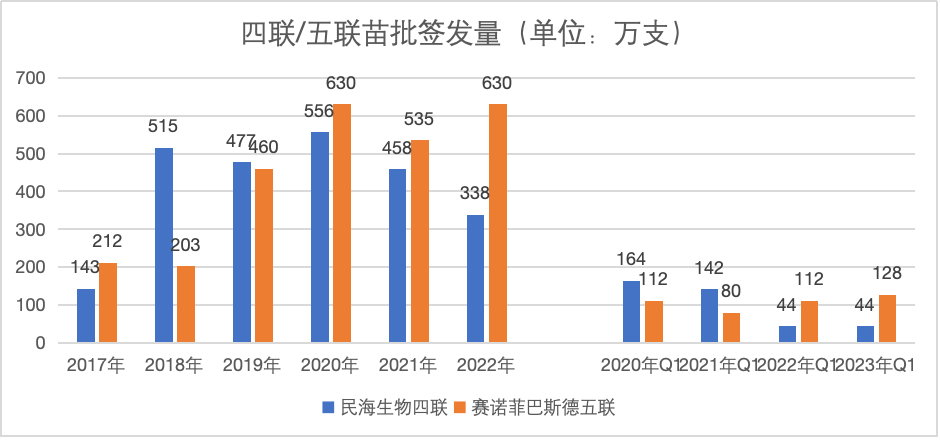
2020至2022年间,国产四联疫苗批签发量逐年递减,2020年为556万支,2021年减少为458万支,而2022年仅有338万支。进口五联疫苗批签发量在这三年间有所波动,2020年为630万支,2021年缩减为535万支,而2022年恢复成为2020年同等水平。
《疫苗生产流通管理规定》与多联多价疫苗
为加强落实《疫苗管理法》项下对于对疫苗的生产、流通管理活动进行规范,国家药监局在2020年和2021年针对《疫苗生产流通管理规定》进行了两次公开征求意见,并在2022年7月8日正式发布该规定。
在《疫苗生产流通管理规定》(下称“规定“)发布之前,我国早期法规规定只有药品生产企业才能持有药品的批准文号,生产联合疫苗的企业必须拥有自己的单苗文号才可以生产联合疫苗,不同疫苗生产企业间(包括同一集团内的不同生产企业)无法合作开发联合疫苗1。
在规定发布之后,疫苗的研发、注册、生产和流通将实行类似于普通药品的上市许可持有人(“持有人”)制度,规定明确了疫苗持有人可提出委托生产申请的适用情形、委托方和受托方需要满足的条件、委托生产的具体流程等细节,为合作研发生产多联多价疫苗提供了可能性2。
审核校对:陈姝,邓添艺,蒋梦露
网页编辑:祖嘉琦
参考文献
- 赵杨升等.我国联合疫苗产业发展现状、问题及对策. 中国医药工业杂志. 2018,49(9). https://xueshu.baidu.com/usercenter/paper/show?paperid=1g2k0cv0kc1002n0we0k0mt0h4658951&site=xueshu_se. Accessed Sep. 22, 2024.
- 国家药品监督管理局.《疫苗生产流通管理规定》. https://www.nmpa.gov.cn/xxgk/fgwj/xzhgfxwj/20220708185734126.html. Accessed Sep. 22, 2024.





