苏格兰是英国(大不列颠及北爱尔兰联合王国,The United Kingdom of Great Britain and Northern Ireland)的政治实体之一,人口约550万(1) ,占英国总人口的8%。苏格兰经济以能源、生命科学和金融服务为核心,贡献了英国国内生产总值的7–8%左右。作为英国重要的经济文化部分,苏格兰在卫生、教育等领域享有高度自治权,并长期实施独立的公共卫生政策(2) 。自2000年以来,苏格兰每年约新增宫颈癌病例320例,且发病人群以年轻女性为主,35–40岁群体发病率最高(3) 。
1.政策背景与发展历程
2007年6月,英国疫苗接种和免疫联合委员会 (Joint Committee on Vaccination and Immunization, JCVI) 向卫生部提出建议,将 HPV 疫苗纳入英国12-13 岁女生的常规免疫接种计划 (4) 。该建议综合考虑了成本效果,基于学校接种的实施便利,校内性教育开始的时间,以及14岁之后感染率增加的证据等多个因素(5, 6) 。同时,基于更新的成本效果模型研究,JCVI建议从2008年9月启动面向 13-17 岁女生的补种运动(7)。
基于JCVI的建议,为了降低 HPV 相关肿瘤发生率,苏格兰国家卫生服务体系(NHS Scotland)于2008年启动 HPV 疫苗接种计划。自2008年9月起,苏格兰为12–13岁(相当于中学二年级)女生提供常规三剂疫苗接种,作为常规免疫接种计划的一部分,年度目标接种人数约25,500人(3, 8)。同时在2008年9月至2011年8月间,为13–17岁女生实施补种项目,目标覆盖约77,000人。该接种计划实施时并未设定HPV疫苗接种的具体目标,但预期的接种率为80%或以上;实际在项目首年和次年,三剂次HPV 疫苗达成的接种率分别为91.4%和90.1%(3,7)。
2.高覆盖率背后的规划与实施
苏格兰HPV 疫苗项目取得显著成效:项目第一年(2008–2009)常规队列女生三剂完成率达91.4%,显著高于英国平均83.5%;次年(2009–2010)仍维持90.1%的高覆盖率(3)。
该项目设计与实施体现了系统化公共卫生的干预模式。规划阶段,通过综合评估决定采用基于学校的接种模式,以提高可及性、效率和监测便捷性(3)。所有在校12–13岁女生均在学校统一组织的接种点完成免疫(9)。针对校外青少年女性,尤其是16岁以上群体,地方卫生委员会可灵活选择全科诊所或专设接种中心进行接种,以确保覆盖高风险群体(3)。
依据 PRINCE2 项目管理框架,本项目设立专职项目经理,负责整体工作的统筹协调与风险管理。为确保项目有效实施,专门设立了五个专项工作组,各自聚焦关键运营领域。工作组成员包括:公共卫生专家、苏格兰健康保护组织 (Health Protection Scotland)、地方卫生委员会、国家支持机构(含数据管理与宣传团队)及苏格兰政府。所有成员均以志愿形式参与工作组工作。工作组会议采取定期机制(通常为每月一次),其频次将根据项目阶段实际需求进行动态调整。为了加强治理与协调,苏格兰政府代表及专职项目经理均参与所有专项工作组的会议活动(3)。
苏格兰采取了分阶段实施策略:常规和补种项目于2008年9月同时启动,补种项目按年龄分层,首年针对16–17岁,次年扩大至13–16岁,历时三年。项目设计充分考虑不同年龄段需求与可行性,明确“难以覆盖群体”,即因社会经济水平较低、地理偏远或就医障碍导致接种率较低的高风险人群,并开展社区动员及流动接种,以缩小差距。
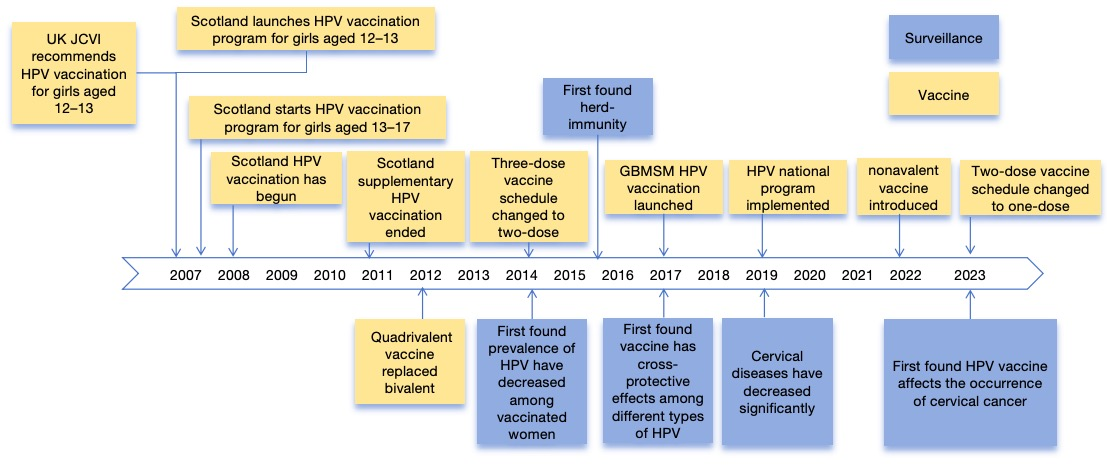
在初期实施完成后,苏格兰于2012年将二价疫苗升级为四价疫苗(兼具生殖器疣保护);2014年将三剂方案调整为两剂;2017年拓展至男同性恋、双性恋及其他男男性行为者(GBMSM);2019年为全国 HPV 疫苗计划;2022年引入九价疫苗,可覆盖约87%的宫颈癌相关 HPV 型别;至2023年,剂次进一步精简为单剂方案(见图1)(3, 10, 11)。
3.苏格兰 HPV 疫苗接种项目的组织架构
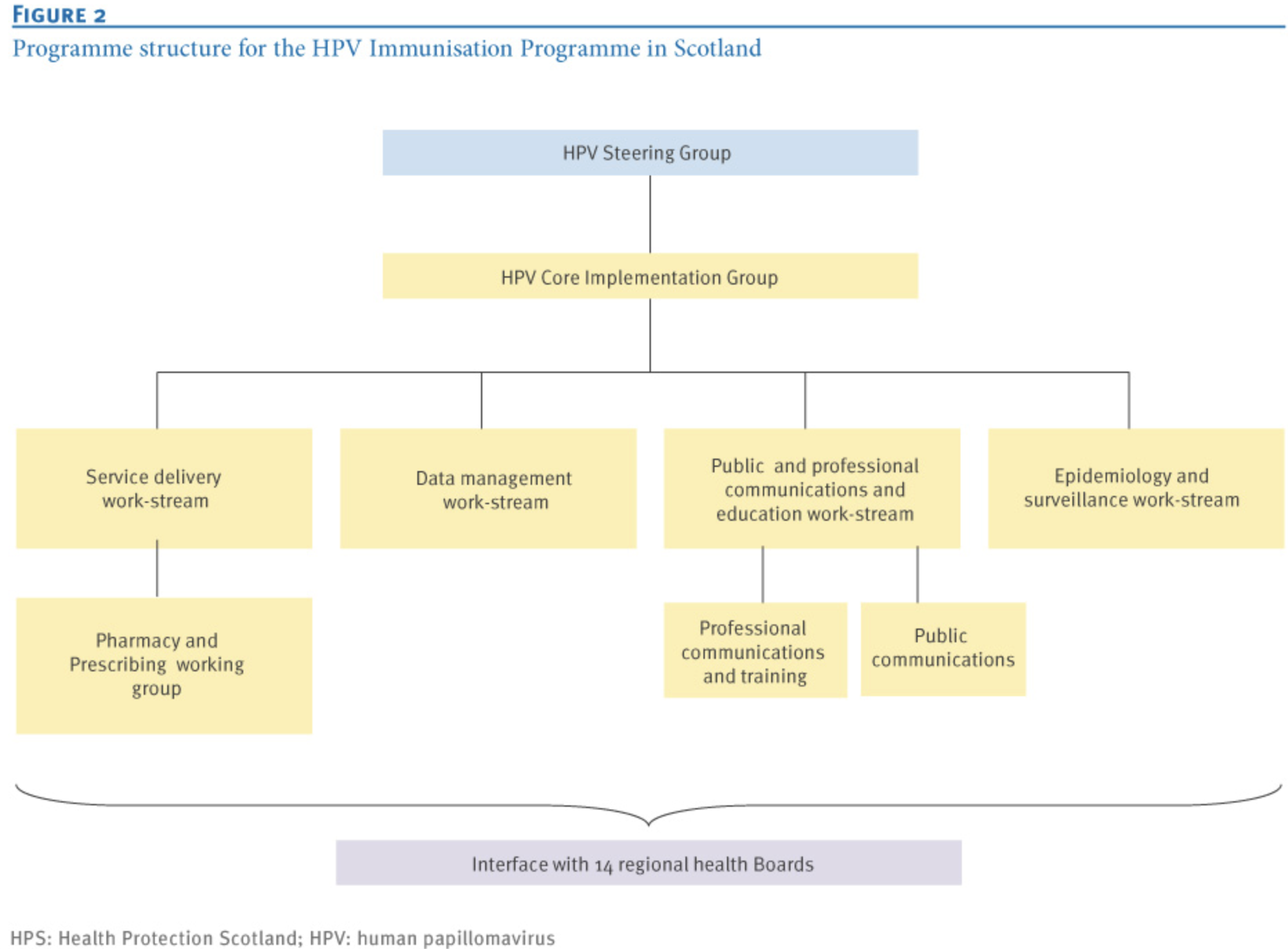
苏格兰的 HPV 疫苗接种项目由一系列专业工作组协同推进,形成了清晰的、多部门协同的组织体系。在国家指导小组下成立了多个工作组,由核心实施工作组(Service Core Implementation Working Group)统筹项目整体执行,其关键利益相关方包括苏格兰政府、苏格兰国家医疗服务机构、地方卫生部门以及相关教育部门等(8),在核心实施工作组的下面包含:
- 服务提供工作组(Service Delivery Workstream):服务提供工作组确保NHS全面统筹HPV疫苗接种准备工作,通过与地方卫生委员会建立协作机制,确保地方免疫服务实施、数据流转及疫苗分发等环节有效衔接。其下设药学与处方工作组(Pharmacy and Prescription Working Group),负责处方指南、采购、储运及法规合规,由 NHS 药学专家领导。
- 数据管理工作组(Data Management Workstream):负责确定目标人群,优化信息系统,保证教育与公共卫生部门的数据互通,由数据科学与流行病学专家组成。
- 宣传与教育工作组(Communication and Educational Workstream):负责面向公众及专业群体的推广事务,具体包括多媒体宣传以及免疫接种人员的培训工作,由健康传播领域的资深专家领衔主持。
- 流行病学与监测工作组(Epidemiology and Surveillance Workstream):负责项目效果评价及长期影响监测工作,并统筹跨区域实验室协作。该工作组核心团队涵盖数据分析师、统计学家及公共卫生专业人员。
此外,各专项工作组通过核心实施团队横向联动,定期(月度)会议以确保各项工作同步推进。战略决策与风险管理则由政府指导小负责,体现了多层级治理结构与跨部门协作的高效机制(3)(见图2)。
3.1服务提供
服务提供工作组确保NHS全面统筹HPV疫苗接种准备工作,通过与地方卫生委员会建立协作机制,确保地方免疫服务实施、数据流转及疫苗分发等环节有效衔接。服务提供工作组在苏格兰政府主导下,既负责评审各卫生委员会的实施方案并推动跨区域最佳实践共享,又重点保障服务覆盖不足人群的公平接种权益,同时协调知情同意等相关事务。该工作组通过与全国基层医疗机构充分协商持续优化服务配置,成员涵盖卫生委员会代表、学校及教育部门代表、学校护士、全科医生、药剂师和相关专项工作组人员,由资深临床公共卫生医师领衔。药学与处方作为服务提供工作组下属机构,提供药剂学咨询,制定安全处方(包括国家级患者群体处方指导)、疫苗供应及管理方案。小组负责确保疫苗采购、储存和分发符合相关法律法规标准,并建立地方订购与配送体系。工作进展与更新通过苏格兰疫苗动态(Scottish Vaccine Update newsletter)通讯发布。成员由药学与物流专家及各卫生委员会代表组成,组长为 NHS 药剂师。
3.2 数据管理
数据管理工作组负责识别符合疫苗接种条件的个体,并协调符合接种程序的召回与追踪机制,其职责是确保从接种邀请到档案记录的数据流畅,这需要对国家信息系统实施技术调整,并生成覆盖率数据。该工作组还负责保障教育部门与公共卫生部门之间的有效数据连接,方便对失学女童进行后续追踪随访。成员包括系统设计、数据分析及流行病学领域的专家,以及来自卫生委员会、教育部门、筛查项目和全科医疗机构的代表。组长由一名具备国家级数据系统管理经验的公共卫生医师担任。
3.3 宣传与教育
宣传与教育工作组负责设计并实施多媒体宣传活动,以提高适龄女生本人、其家长、教育者及医疗提供者对 HPV 疫苗的认可度。专业传播手段包括利益相关方简报、定期向服务提供者发送专业信函,以及对免疫护士的专项培训。针对离校人群,还曾启用“粉色宣传车”开展现场宣教。团队成员来自传播学、培训、流行病学、学校教育及 NHS 24 小时热线等多个领域,由 NHS 资深健康传播专家担任组长。
3.4 流行病学与监测
流行病学与监测工作组负责开发疫苗覆盖率与安全性评估工具,并监测疫苗对高危 HPV 感染、宫颈癌及癌前病变的影响,以便为筛查、HPV 检测与免疫策略的平衡提供循证指导。为保障跨区域监测一致性,已创立苏格兰国家 HPV 参考实验室,并与英格兰健康保护署(现为英格兰国家卫生防护研究所)合作。成员包括流行病学家、实验室代表、统计学家,以及数据管理组和卫生委员会专家,组长为苏格兰卫生防护部的高级临床负责人。
3.5 项目协调与监督
各专项工作组的进展通过核心实施团队(月度会议)进行统筹协调,该团队由各工作组组长、项目经理及苏格兰政府代表组成。政府任命的指导小组负责全程监督项目执行,审批战略决策,并在关键阶段委托第三方进行“节点审查(Gateway Reviews)”以评估风险、治理与流程。该指导小组每季度召开一次会议,成员包括来自教育、公共卫生、学校及患者权益倡导领域的代表,其主席由不直接参与项目管理的卫生委员会高级管理人员担任。
4.疫苗接种的积极影响
苏格兰是全球首批推行二价和四价HPV疫苗的国家之一。这两种疫苗均能预防高危型HPV 16和18感染——该类病毒与宫颈上皮内瘤变(CIN)存在强相关性。研究表明,上述疫苗可诱导持久的中和抗体应答并有效预防相关病变。其中,二价疫苗对与HPV 16/18相关的其他高危型(如31、33和45型)具有交叉保护作用;四价疫苗亦对HPV 31和33型产生部分交叉保护(12, 13)。此外,苏格兰监测数据显示:2013年未接种女性群体中HPV 16/18感染率显著低于2009年水平(21.2% vs. 30.0%),印证了疫苗接种项目引发的群体免疫效应(14)。基于人群的监测数据进一步表明,HPV疫苗接种与年轻女性低级别(CIN1)及高级别宫颈上皮内瘤变发病率下降存在强相关性 (15)。在苏格兰完成三剂次二价疫苗接种的群体中,CIN2发病率降低50%,CIN3发病率下降55%。值得注意的是,这些显著成效已在补种队列中得到验证,预示着在常规接种人群中效果可能更为显著 (14) 。
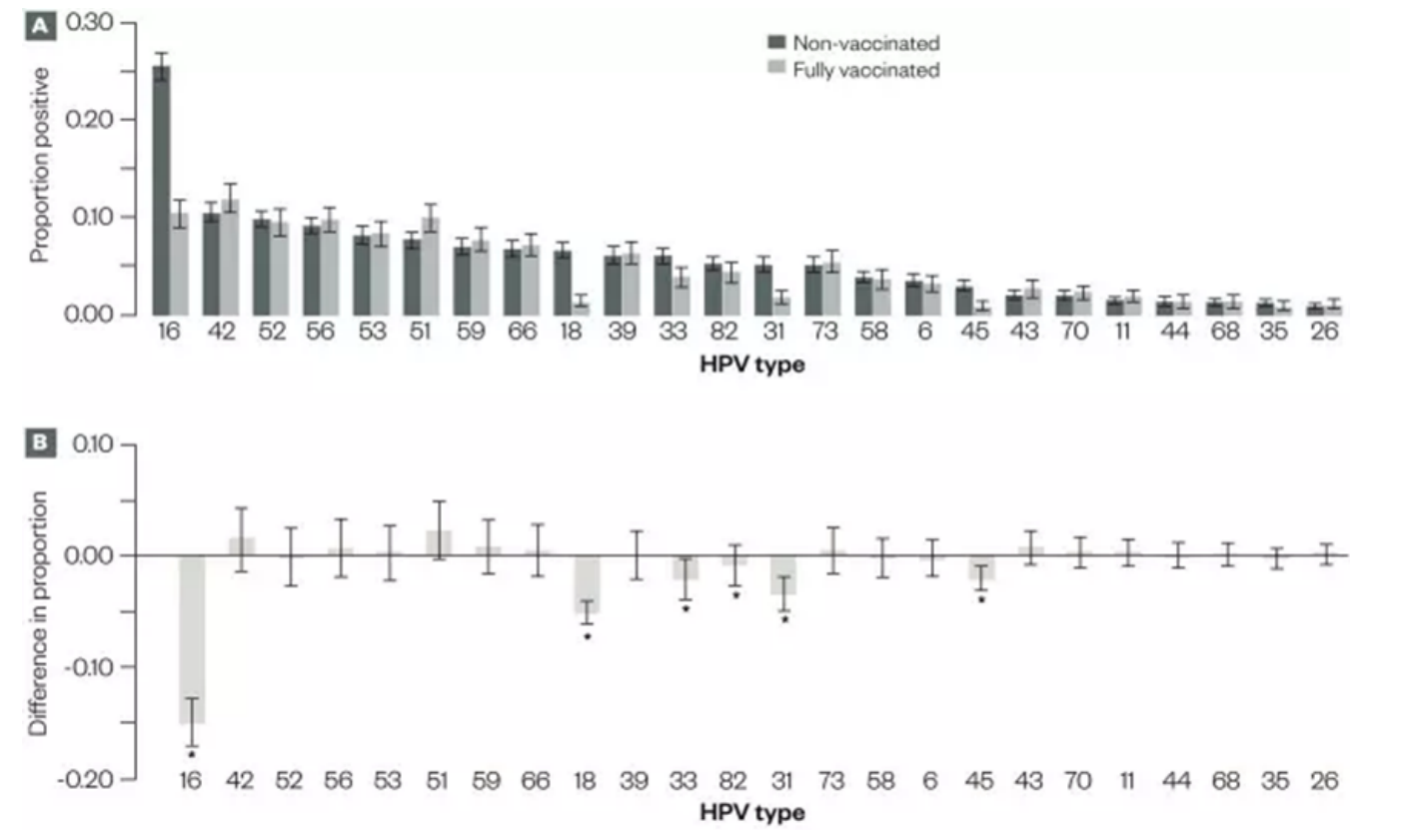
研究结果进一步证实了 HPV 疫苗在预防宫颈疾病和癌症方面的显著保护作用。一项发表在英国医学杂志(British Medical Journal)上的回顾性人群研究显示,在12–13岁接种双价 HPV 疫苗的女孩,到20岁时,CIN3或更严重病变的风险降低了89%,CIN2+ 风险降低了88%,CIN1 风险降低了79%;此外,未接种女性也观察到了宫颈病变风险的下降(16)。
另一项发表于柳叶刀的研究结果显示,12–13岁接种 HPV 疫苗女生的宫颈癌发病率降低了87%(17)。根据最新的 NHS 研究,截至目前,在这一年龄段完成全程接种的女性中尚未发现宫颈癌病例(10),进一步证明了该疫苗的高度预防效果。上述研究为 HPV 疫苗在宫颈癌预防中的有效性提供了直接证据,强调了早期接种的重要性。更多细节见“图1”。
5. 持续监测与改进
为保障项目质量,苏格兰建立了多维度的全面监测体系,包括:
- 建立由苏格兰学校健康监测项目(Scottish Child Health Surveillance Programme – Schools)、苏格兰学前健康监测项目(Child Health Surveillance Programme – Pre school)和苏格兰免疫召回系统(Scottish Immunisation Recall System)组成的免疫和监测系统(7)。
- 调查家长、儿童、教育工作者及医务人员对 HPV、宫颈癌及疫苗的认知和态度,评估面向公众宣传教育材料的可接受性;
- 开发低成本、简便可靠的 HPV 检测方法,以监测目标接种人群的感染率(18-20);
- 在免疫前测定未接种人群的基线感染率及流行基因型(21);
- 建立覆盖率、安全性及早期效果监测系统,通过筛查分析妇女 HPV 感染率变化,评估初期免疫影响;
- 比较筛查参与者与非参与者的人口学和行为特征(22),评估监测样本的代表性,确保结果在苏格兰女性群体中具有广泛适用性。
6.总结
尽管项目已取得显著成效,苏格兰卫生部门仍持续监测 HPV 疫苗策略效果,并依据最新研究和数据不断优化,以保持高覆盖率和预防效果。苏格兰的经验表明,系统化规划与多部门协作能够带来显著公共卫生收益,为其他地区提供了宝贵借鉴。
文章撰稿:吴迪
编译整理:朱姿颐
编辑排版:李睿彤
参考文献
1. G. Y. Ho, R. Bierman, L. Beardsley, C. J. Chang, R. D. Burk, Natural history of cervicovaginal papillomavirus infection in young women. N Engl J Med 338, 423-428 (1998).
2. S. Government, Scottish economic outlook (2024).
3. A. Potts et al., High uptake of HPV immunisation in Scotland–perspectives on maximising uptake. Euro Surveill 18 (2013).
4. D. o. H. (DH), Joint Committee on Vaccination and Immunisation (JCVI). JCVI meeting minutes of the meeting held on Wednesday 20 June 2007 at 10.30am. [Accessed 25 Sep 2013]. (2013).
5. M. Jit, Y. H. Choi, W. J. Edmunds, Economic evaluation of human papillomavirus vaccination in the United Kingdom. Bmj 337, a769 (2008).
6. J. C. o. V. a. Immunisation (2007) Minutes of the meeting held on Wednesday 20 June 2007 at 10.30am.
7. T. S. Government (2008) Public Health and Wellbeing Directorate. Implementation of Immunisation Programme: Human Papilloma Virus (HPV) Vaccine – Project Update including the Catch Up Campaign. .
8. T. S. Government. (2007) Public Health and Wellbeing Directorate. Implementation of Immunisation Programme: Human Papillomavirus (HPV) Vaccine.
9. K. Sinka et al., Achieving high and equitable coverage of adolescent HPV vaccine in Scotland. J Epidemiol Community Health 68, 57-63 (2014).
10. P. H. Scotland (2024) No cervical cancer cases detected in vaccinated women following HPV immunisation.
11. T. J. Palmer et al., Invasive cervical cancer incidence following bivalent human papillomavirus vaccination: a population-based observational study of age at immunization, dose, and deprivation. JNCI: Journal of the National Cancer Institute 116, 857-865 (2024).
12. J. Paavonen et al., Efficacy of human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine against cervical infection and precancer caused by oncogenic HPV types (PATRICIA): final analysis of a double-blind, randomised study in young women. Lancet 374, 301-314 (2009).
13. S. N. Tabrizi et al., Assessment of herd immunity and cross-protection after a human papillomavirus vaccination programme in Australia: a repeat cross-sectional study. Lancet Infect Dis 14, 958-966 (2014).
14. C. Pharmacist, The impact of the human papillomavirus vaccine in Scotland: a changing landscape. Pharmaceutical Journal 9 (2017).
15. K. G. Pollock et al., Reduction of low- and high-grade cervical abnormalities associated with high uptake of the HPV bivalent vaccine in Scotland. Br J Cancer 111, 1824-1830 (2014).
16. T. Palmer et al., Prevalence of cervical disease at age 20 after immunisation with bivalent HPV vaccine at age 12-13 in Scotland: retrospective population study. Bmj 365, l1161 (2019).
17. M. Falcaro et al., The effects of the national HPV vaccination programme in England, UK, on cervical cancer and grade 3 cervical intraepithelial neoplasia incidence: a register-based observational study. Lancet 398, 2084-2092 (2021).
18. W. Forson et al., High-risk HPV mRNA testing on self-samples offered to those who do not attend for organised cervical screening – real world data from the Dumfries and Galloway region in Scotland. J Clin Virol 175, 105734 (2024).
19. K. Cuschieri et al., Urine testing as a surveillance tool to monitor the impact of HPV immunization programs. J Med Virol 83, 1983-1987 (2011).
20. K. Cuschieri et al., Effect of HPV assay choice on perceived prevalence in a population-based sample. Diagn Mol Pathol 22, 85-90 (2013).
21. M. C. O’Leary et al., HPV type-specific prevalence using a urine assay in unvaccinated male and female 11- to 18-year olds in Scotland. Br J Cancer 104, 1221-1226 (2011).
22. K. Sinka et al., Acceptability and response to a postal survey using self-taken samples for HPV vaccine impact monitoring. Sex Transm Infect 87, 548-552 (2011).





