肺炎球菌(Streptococcus pneumoniae,Spn)是于1881年发现的柳叶刀形革兰氏阳性兼性厌氧细菌[1]。Spn是一种重要的条件致病菌,常定植在人的鼻咽部,高达27%-65%的儿童和<10%的成人是肺炎链球菌的携带者[1,2]。一般情况下并不致病,具体取决于人群特征和定植环境的变化[1]。
Spn广泛分布于自然界,人类是其唯一宿主。Spn在人与人之间传播,一般经由呼吸道飞沫或由在上呼吸道的定植菌导致感染,其感染通常在冬季和早春更为常见[1]。尽管关于肺炎球菌性疾病的传染期尚不清楚,但据推测,只要呼吸道分泌物中存在病原体,就有发生疾病传播的可能[3]。
肺炎球菌性疾病(Pneumococcal disease, PD)是由Spn引起的一组感染性疾病的总称,可根据Spn感染部位不同,分为侵袭性肺炎球菌性疾病(Invasive pneumococcal disease, IPD)和非侵袭性肺炎球菌性疾病(Non-invasive pneumococcal disease, NIPD)[4]。NIPD远比IPD常见,但因很少进行病原学检查导致常无法明确系肺炎链球菌感染;IPD虽少见,但症状更重,致死风险高[5]。
肺炎链球菌迁移到无菌组织和器官是所有肺炎球菌疾病的主要原因[6]。常在鼻咽部定植的肺炎链球菌,如果不能被免疫系统清除,这种细菌可以到达其他组织器官或下呼吸道,从而出现侵袭性感染[7]。常见的IPD包括肺炎、菌血症和脑膜炎等。
研究表明,增加IPD患病风险的因素包括:疾病或药物导致免疫功能低下、功能性或解剖性无脾、慢性心脏疾病、肺部疾病(包括哮喘)、肝脏或肾脏疾病、吸烟、酒精中毒、脑脊液漏、人工耳蜗,以及处于托幼机构等集体单位的儿童[8]。
现有已知近100种血清型的Spn,其中大部分可以引起疾病,但全世界约有62%的IPD是由10种最常见的血清型引起[6]。携带者中最常见的Spn致病血清型也是导致感染的主要血清型。尽管携带Spn不一定会导致疾病,但它是发生PD的重要前提[9]。不同的血清型可能会倾向性的引起不同的疾病或状态,如无症状定植、脑膜炎、肺炎等。
图1:肺炎球菌导致的1-59月龄儿童的死亡数
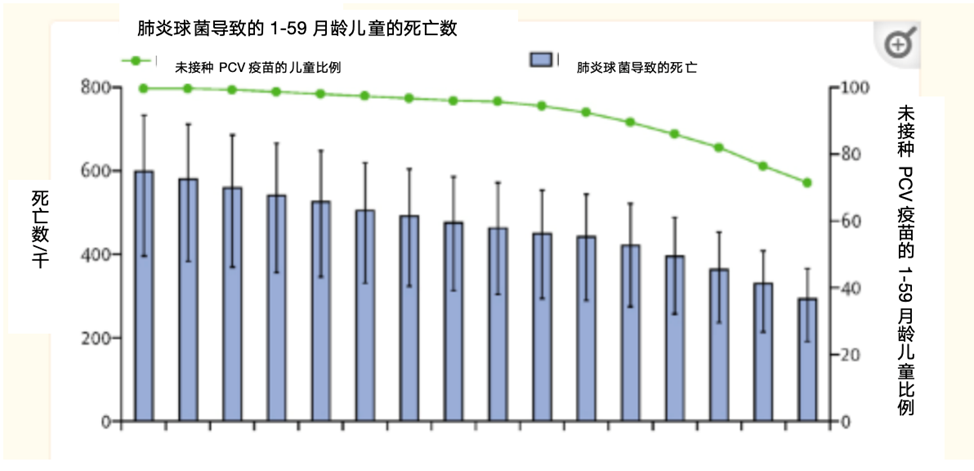
(图片来源:Wahl, B., O’Brien, K. L., Greenbaum, A., Majumder, A., Liu, L., Chu, Y., … & Cohen, A. L. (2018). Burden of Streptococcus pneumoniae and Haemophilus influenzae type b disease in children in the era of conjugate vaccines: global, regional, and national estimates for 2000–15. The Lancet Global Health, 6(7), e744–e757.)
Spn致病血清型分布在地理区域、年龄和临床表现上有一定的差异。全球5岁以下儿童中最常见的七种血清型为1, 5, 6A, 6B, 14, 19F, 23F,覆盖各地区IPD的一半以上[10]。2010年发表的一项系统综述研究描述了1980-2007年全球5岁以下IPD患儿的血清型分布情况(图2)[10]。在东南亚地区的全人群中,IPD报告病例中最常见的血清型为血清组19(16.2%)、6(14.6%)、23(12.5%)和血清型14(9.2%)、1(5.7%)、3(4.0%)[11]。在中国,1980-2008年间的文献系统回顾研究表明,14、19A和19F血清型是中国<5岁儿童肺炎和脑膜炎病例中最常见的血清型[12];此外,有研究发现我国大陆地区儿童IPD的常见血清型为19A,19F,14,23F和6B[13]。
图2: 世界卫生组织地区不同年龄组人群PCV疫苗上市前疫苗覆盖的血清型的分布情况。
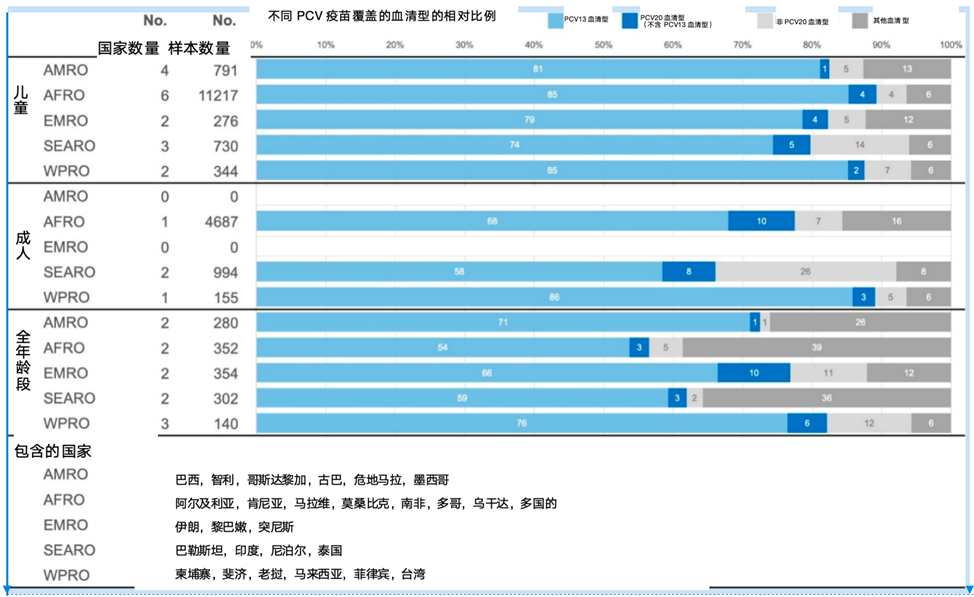
(图片来源:Fletcher, M. A., Daigle, D., Siapka, M., Baay, M., Hanquet, G., & Morales, G. D. C. (2024). Serotype distribution of invasive pneumococcal disease from countries of the WHO Africa, Americas, Eastern Mediterranean, South-East Asia, and Western Pacific regions: A systematic literature review from 2010 to 2021. Frontiers in Public Health, 12.)
表1:不同价次PCV疫苗纳入免疫规划后,PCV血清型的分布情况
| WHO区域 AMRO | 国家/地区 | 年龄组 | 时期 | 纳入时间 | 研究 ID | 研究时期 | PCV13血清型 | PCV20血清型(不包括PCV13血清型) | 非PCV20血清型 | 其他血清型 | 总数 |
| % | % | % | % | N | |||||||
| 阿根廷 | 儿童 | PCV | PCV13(2012) | 3860 | 2012-2013 | 62.7 | 11.9 | 7.5 | 13.4 | 67 | |
| 2012-2013 | 79.4 | 20.6 | 563 | ||||||||
| 1270 | 2015-2017 | 34.3 | 21.0 | 32.7 | 12.0 | 434 | |||||
| 成人 | PCV-hv | PCV13(2012) | 1245 | 2013-2017 | 43.1 | 27.6 | 4.6 | 24.8 | 791 | ||
| 巴西 | 儿童 | PCV-hv | PCV10(2010) | 1828 | 2010-2012 | 72.0 | 9.8 | 17.8 | 0.3 | 325 | |
| 450 | 2011-2015 | 51.6 | 48.4 | 62 | |||||||
| 1270 | 2015-2017 | 46.7 | 18.1 | 29.7 | 5.4 | 441 | |||||
| 成人 | PCV-hv | PCV10(2010) | 197 | 2013-2015 | 51.0 | 23.5 | 7.6 | 02 | |||
| 全年龄段 | PCV-hv | PCV10(2010) | 748 | 2010-2012 | 61.6 | 14.5 | 19.5 | 4.4 | 159 | ||
| 121 | 2014-2015 | 47.5 | 19.9 | 25.0 | 7.4 | 1630 | |||||
| 120 | 2017-2019 | 44.6 | 7.2 | 36.8 | 1.5 | 2402 | |||||
| 智利 | 儿童 | PCV-hv | PCV10(2011) | 1127 | 2012-2012 | 60.4 | 1.1 | 38.5 | 91 | ||
| 1270 | 2015-2017 | 52.7 | 4.6 | 28.2 | 4.5 | 404 | |||||
| 哥伦比亚 | 儿童 | PCV-hv | PCV10(2011) | 1270 | 2015-2017 | 66.8 | 4.8 | 26.1 | 3.1 | 352 | |
| 成人 | PCV-hv | PCV10(2011) | 4034 | 2012-2019 | 48.1 | 4.2 | 37.7 | 310 | |||
| 全年龄段 | PCV-hv | PCV10(2011) | 3267 | 2012-2017 | 56.9 | 11.4 | 31.6 | 0.1 | 842 | ||
| 多米尼加共和国 | 儿童 | PCV-hv | PCV13(2013) | 1270 | 2015-2017 | 67.2 | 3.4 | 19.0 | 10.3 | 58 | |
| 全年龄段 | PCV-hv | PCV13(2013) | 3480 | 2013-2016 | 897 | 10.3 | 39 | ||||
| 墨西哥 | 儿童 | PCV-hv | PCV13(2011) | 270 | 2015-2017 | 41.2 | 18.3 | 32.0 | 8.5 | 153 | |
| 巴拉圭 | 儿童 | PCV-hv | PCV10(2011) | 1270 | 2015-2017 | 679 | 10.1 | 13.8 | 8.3 | 109 | |
| 秘鲁 | 儿童 | 过渡期 | PCV7(2009 | 2009-2011 | 84.5 | 10.3 | 58 | ||||
| 全年龄段 | 过渡期 | PCV7(2009) | 2136 | 2010-2011 | 64.6 | 15.2 | 15.2 | 2.5 | 79 | ||
| 乌拉圭 | 儿童 | PCV-hv | PCV13(2010) | 1270 | 2015-2017 | 43.7 | 9.5 | 29.9 | 6.9 | 87 | |
| 全年龄段 | PCV-hv | PCV13(2010) | 348 | 2011-2012 | 46.1 | 53.9 | 356 | ||||
| 委内瑞拉 | 儿童 | 混合期 | pre-PCV,PCV13(2014) | 1270 | 2006-2017 | 90.6 | 9.4 | 309 | |||
| AFRO | 布基纳法索 | 儿童 | PCV-hv | PCV13(2013) | 3356 | 2014a | 88.0 | 12.0 | 25 | ||
| 2017b | 50.0 | 7.1 | 42.9 | 14 | |||||||
| 全年龄段 | PCV-hv | PCV13(2013) | 2320 | 2014-2015 | 72.7 | 8.1 | 3.3 | 15.8 | 377 | ||
| 3355 | 2016-2017 | 56.0 | 0.5 | 2.0 | 41.4 | 739 | |||||
| 喀麦隆 | 儿童 | 混合期 | pre-PCV,PCV13(2011) | 1493 | 2010-2016 | 55.2 | 27.6 | 17.2 | 29 | ||
| PCV-hv | PCV13(2011) | 2536 | 2015-2018 | 35.8 | 17.0 | 30.2 | 17.0 | 53 | |||
| 埃塞俄比亚 | 全年龄段 | PCV-hv | PCV10(2011) | 2018-2019 | 37.1 | 5.7 | 28.6 | 28.6 | 35 | ||
| 冈比亚 | 儿童 | 混合期 | Pre-PCV,PCV7(2009), PCV13(2011) | 2575 | 1995-2016 | 63.1 | 17.7 | 19.2 | 203 | ||
| 加纳 | 全年龄段 | PCV-hv | PCV13(2012) | 2445 | 2015-201 | 69.5 | 0.2 | 3.4 | 16.9 | 59 | |
| 1497 | 2015-2017 | 71.5 | 28.5 | 137 | |||||||
| 肯尼亚 | 儿童 | PCV-hv | PCV10(2011) | 400 | 2012-2016 | 26.8 | 73.2 | 82 | |||
| 马达加斯加 | 儿童 | PCV-hv | PCV10(2012) | 4041 | 2013-2018 | 19.5 | 1.1 | 37.9 | 41.4 | 87 | |
| 马拉维 | 儿童 | 混合期 | Pre-PCV,PCV13(2011) | 2575 | 1995-2016 | 73.0 | 6.6 | 20.4 | 226 | ||
| 全年龄段 | 多时期 | Pre-PCV,PCV13(2011) | 1407 | 2006-2018 | 54.5 | 45.5 | 1594 | ||||
| 莫桑比克 | 儿童 | PCV-hv | PCV10(2013) | 785 | 2013-2014 | 62.0 | 2.0 | 36.0 | 50 | ||
| 2870 | 2013-2015 | 71.0 | 29.0 | 69 | |||||||
| 695 | 2014-2015 | 70.0 | 3.3 | 20.0 | 6.7 | 30 | |||||
| 尼日尔 | 全年龄段 | PCV-hv | PCV13(2014) | 2958 | 2016-2018 | 42.4 | 5.3 | 4.1 | 38.2 | 70 | |
| 尼日利亚 | 儿童 | 混合期 | Pre-PCV,PCV10(2014) | 1073 | 2010-2016 | 50.0 | 3.6 | 46.4 | 28 | ||
| 塞内加尔 | 儿童 | 混合期 | Pre-PCV,PCV13(2013) | 3365 | 2010-2016 | 91.4 | 6.9 | 58 | |||
| 南非 | 儿童 | PCV-hv | PCV13(2011) | 2575 | 2013-2014 | 28.2 | 31.6 | 39.9 | 0.3 | 291 | |
| 全年龄段 | PCV-hv | PCV13(2011) | 3614 | 2012 | 53.6 | 20.4 | 2.3 | 3.9 | 1631 | ||
| 多哥 | 儿童 | PCV-hv | PCV13(2014) | 1111 | 2014-2016 | 60.0 | 40.0 | ||||
| 赞比亚 | 儿童 | PCV-hv | PCV10(2013) | 4033 | 2014-2019 | 52.0 | 2.0 | 50 | |||
| 多国 | 儿童 | 混合期 | Pre-PCV,PCV-hv | 3261 | 2010-2016 | 33.5 | 4.1 | 62.4 | 370 | ||
| EMRO | 科威特 | 全年龄段 | PCV-hy | PCV13(2010) | 2771 | 2010-2013 | 28.9 | 26.7 | 33.3 | 1.1 | 45 |
| 摩洛哥 | 儿童 | PCV-hv | PCV13(2011),PCV10 2012) | 807 | 2011-2014 | 95.9 | 4.1 | 68 | |||
| 阿曼 | 儿童 | PCV-hv | PCV13(2012) | 1290 | 2014-2016 | 25.7 | 22.9 | 51.4 | 35 | ||
| 成人 | PCV-hv | PCV13(2012) | 1290 | 2014-2016 | 40.0 | 3.3 | 51.7 | 60 | |||
| 全年龄段 | PCV-hv | PCV13(2012) | 1290 | 2014-2016 | 32.4 | 8.1 | 59.5 | 37 | |||
| 巴基斯坦 | 儿童 | PCV-hv | PCV10(2012) | 916 | 2013-2017 | 21.7 | 78.3 | 92 | |||
| 全年龄段 | 混合期 | Pre-PCV,PCV10(2012) | 3275 | 2005-2013 | 42.3 | 5.4 | 14.4 | 37.8 | 111 | ||
| 卡塔尔 | 全年龄段 | 过渡期 | PCV7(2005) | 302 | 2005-2009 | 77.9 | 7.4 | 12.3 | 2.5 | 122 | |
| 沙特阿拉伯 | 儿童 | 混合期 | PCV7(2009),PCV13 (2010) | 19 | 2009-2012 | 84.6 | 2.6 | 6.4 | 6.4 | 78 | |
| 全年龄段 | 混合期 | Pre-PCV,PCV7(2009), PCV13(2010) | 2772 | 2000-2016 | 91.7 | 7.9 | 9.0 | 8.7 | 277 | ||
| WPRO | 柬埔寨 | 儿童 | 混合期 | Pre-PCV,PCV13(2015) | 3514 | 2012-2018 | 86.4 | 13.6 | 22 | ||
新加坡 | 成人 | PCV-hv | PCV13(2011) | 554 | 2012-2017 | 71.4 | 1.1 | 12.7 | |||
| 全年龄段 | 过渡期 | Pre-PCV,PCV13(2011) | 689 | 1997-2013 | 70.5 | 7.4 | 16.9 | 5.2 | 757 | ||
| 中国台湾 | 儿童 | 过渡期 | PCV7(2005)/PCV13 (2015)c | 191 | 2013-2014 | 80.5 | 5.5 | 13.9 | 36 | ||
| PCV-hv | PCV13(2015) | 2590 | 2015-2017 | 39.0 | 9.3 | 51.7 | 205 | ||||
| 成人 | 混合期 | PCV7(2005)/PCV13 2015) c | 599 | 2011-2015 | 66.0 | 1.3 | 18.0 | 4.7 | 50 | ||
| PCV-hv | PCV13(2015) | 189 | 2017-2020 | 44.7 | 9.7 | 41.8 | 3.8 | 237 | |||
| 全年龄段 | 过渡期 | PCV7(2005)/PCV13 (2015) c | 3399 | 2012-2014 | 76.9 | 7.7 | 15.4 | 1.0 | 104 | ||
| 混合期 | PCV7(2005)/PCV13 2015) c,PCV13(2015) | 182 | 2013-2017 | 57.8 | 17.5 | 23.8 | 1.0 | 206 | |||
| PCV-hv | PCV13(2015) | 3702 | 2016-2018 | 44.4 | 16.2 | 33.3 | 6.1 | 99 | |||
| PCV13:和PCV7均覆盖的血清型:4, 6B, 9V, 14, 19F, 18C, 23;PCV13相比PCV7额外覆盖的血清型:1, 5, 7F, 3, 6A, 6A/6B, 19A PCV20: PCV20(22F, 33F, 8, 10A, 11A, 12F, 15B, 15C, 15B/C, 15B/15C). 非PCV20: 指PPSV23-特异的(2, 9N, 17F, 20, 20A, 20B)和NVST. 非疫苗血清型:不可区分的,无法确认的血清型. PCV-hv:采用更高价次的PCV疫苗时期,例如:PCV10或PCV13作为国家免疫规划中的最新应用的疫苗 *从百分比数字中的数据提取,百分比之和可能不总是等于100%. a Hounde和Kaya地区. b Titao地区. c大龄儿童补种 (图片来源:Fletcher, M. A., Daigle, D., Siapka, M., Baay, M., Hanquet, G., & Morales, G. D. C. (2024). Serotype distribution of invasive pneumococcal disease from countries of the WHO Africa, Americas, Eastern Mediterranean, South-East Asia, and Western Pacific regions: A systematic literature review from 2010 to 2021. Frontiers in Public Health, 12.) | |||||||||||
目前上市的疫苗包括肺炎球菌多糖疫苗(Pneumococcal polysaccharide vaccine,PPV)和肺炎球菌多糖结合疫苗(Pneumococcal conjugate vaccine,PCV),涵盖了导致PD最常见的血清型,不同的疫苗所覆盖的血清型有所不同(图3)。
图3:肺炎链球菌相关疫苗覆盖的血清型
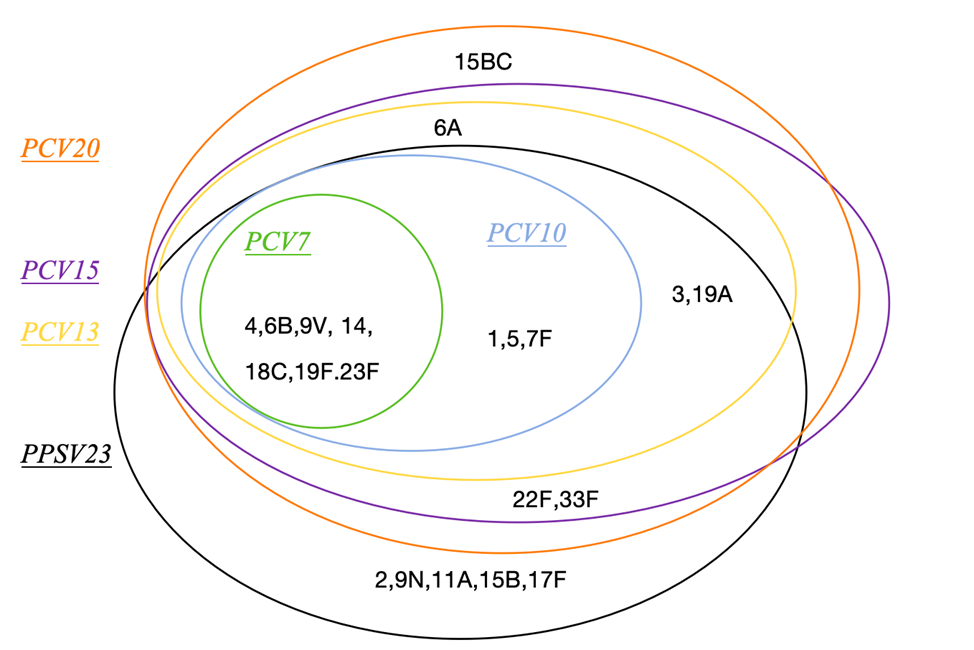
审核校对:李周蓉 潘张旸
图表编辑:张翯昱
网页编辑:祖嘉琦
参考文献
- Weiser, J.N., Ferreira, D.M. & Paton, J.C. Streptococcus pneumoniae: transmission, colonization and invasion. Nat Rev Microbiol 16, 355-367 (2018). https://doi.org/10.1038/s41579-018-0001-8
- Yahiaoui RY, den Heijer CDj, van Bijnen EM, Paget WJ, Pringle M, Goossens H, Bruggeman CA, Schellevis FG, Stobberingh EE; APRES Study Team. Prevalence and antibiotic resistance of commensal Streptococcus pneumoniae in nine European countries. Future Microbiol. 2016 Jun;11:737-44. doi: 10.2217/fmb-2015-0011. Epub 2016 May 18. PMID: 27191588.
- CDC. Pinkbook: Pnumococcal Disease. https://www.cdc.gov/vaccines/pubs/pinkbook/pneumo.html#epidemiology. Accessed December 31, 2021.
- 中华预防医学会.中华预防医学会疫苗与免疫分会.肺炎球菌性疾病免疫预防专家共识(2020版).中华流行病学杂志,2020,41(12):1945-1979.DOI: 10.3760/cma.j.cn112150-20201110-01353
- 姚开虎. 中国肺炎链球菌性疾病负担概况.中华医学杂志,2020,100 (42): 3363-3366. DOI: 10.3760/cma.j.cn112137-20200825-02462
- Brooks Lavida R K,Mias George I. Streptococcus pneumoniae’s Virulence and Host Immunity: Aging, Diagnostics, and Prevention.Front Immunol, 2018, 9: 1366.DOI: 10.3389/fimmu.2018.01366
- CDC. Pneumococcal Disease: Risk Factors for Clinicians. https://www.cdc.gov/pneumococcal/clinicians/risk-factors.html. Accessed December 31, 2021.
- 国家呼吸系统疾病临床医学研究中心, 国家儿童医学中心, 中华医学会儿科学分会呼吸学组, 等.中国儿童肺炎链球菌性疾病诊断、治疗和预防专家共识 [J] . 中华实用儿科临床杂志,2020,35 (07): 485-505. DOI: 10.3760/cma.j.cn101070-20200306-00329
- CDC. Pneumococcal Disease Transmission: For Clinicians. https://www.cdc.gov/pneumococcal/clinicians/transmission.html. Accessed December 31, 2021.
- Johnson HL, Deloria-KM, Levine OS et al. Systematic evaluation of serotypes causing invasive pneumococcal disease among children under five: the pneumococcal global serotype project. PLoS Med. 2010,7(10):e1000348. DOI: 10.1371/journal.pmed.1000348.
- Jauneikaite, E., Jefferies, J. M., et al. Prevalence of Streptococcus pneumoniae serotypes causing invasive and non-invasive disease in Southeast Asia: a review. Vaccine. 2012,30(24), 3503–3514.
- Chen Y, Deng W, Wang SM, et al. Burden of pneumonia and meningitis caused by Streptococcus pneumoniae in China among children under 5 years of age: a systematic literature review[J]. PLoS One, 2011, 6(11): e27333. DOI: 10.1371/journal.pone.0027333
- Men, W., Dong, Q., Shi, W. et al. Serotype distribution and antimicrobial resistance patterns of invasive pneumococcal disease isolates from children in mainland China—a systematic review. Braz J Microbiol.2020,51(2): 665–672. https://doi.org/10.1007/s42770-019-00198-9





