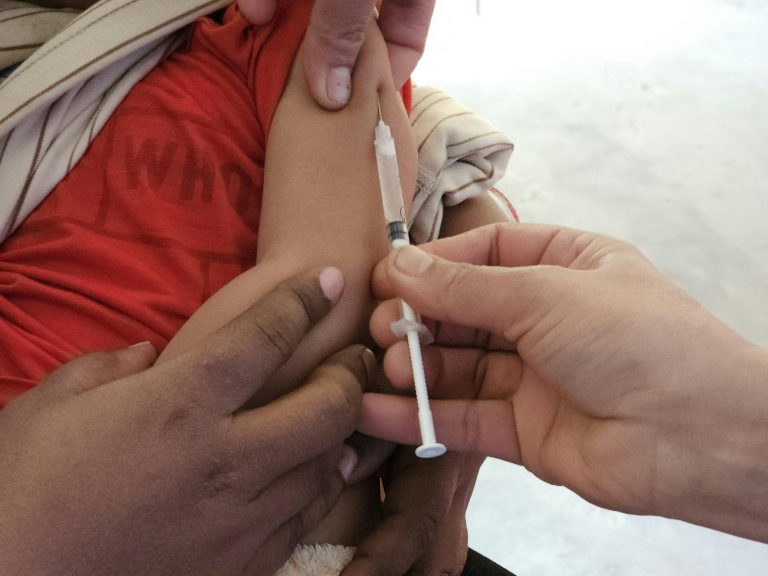
VaxLab为HPV疫苗纳入免规提供关键支持
9月11日,国家卫生健康委副主任、国家疾控局局长沈洪兵在国新办新闻发布会上介绍,今年年内国家将推出面向适龄女生的人乳头瘤病毒(HPV)疫苗接种服务,并且将HPV 疫苗纳入国家免疫规划,保护女性健康。随着这一政策调整的正式宣布,适龄女生将受益于免费接种政策。这也是中国自2008年以来,再次对国家免疫规划扩容。



Vaccines特刊征稿:免疫接种与公共卫生策略
本期特刊由VaxLab疫苗交付研究创新实验室主任汤胜蓝教授、中国疾病预防与控制中心免疫规划高级顾问Lance Rodewald博士,以及杜克-新加坡国立大学全球健康研究所全球健康评估副教授Taufique Joarder担任客座编辑。欢迎广大读者及合作伙伴积极投稿,包括原创研究文章、系统综述和案例研究,探讨新型疫苗引入的挑战,并鼓励创新性的融资和国家免疫规划管理方法。


VaxLab在世卫网站发布东盟及南盟国家免疫规划比较研究报告
VaxLab 近日在世界卫生组织亚太卫生系统和政策观察站发布了东盟及南盟 13 国免疫规划比较研究报告,并于2 月 10 日在新加坡举办研讨会,由新保集团-杜克新加坡国立大学全球健康研究所和亚太免疫联盟联合主办




VaxLab在BMC子刊发布国家免疫规划研究特辑
昆山杜克大学疫苗交付研究创新实验室(Innovation Lab for Vaccine Delivery Research,VaxLab)日前在BMC Infectious Disease of Poverty上发布了“推进中国的国家免疫规划:提高其有效性和可持续性” 系列专题研究特辑。
策略简报
学术成果

缩小免疫差距:克服东南亚和南亚新疫苗引入的障碍
本文由昆山杜克大学疫苗交付研究创新实验室(VaxLab)发表于Vaccine。文章系统比较了东南亚和...

上海市13价肺炎球菌结合疫苗(PCV13)与轮状病毒疫苗同时接种的安全性与成本分析
本文由复旦大学王伟炳教授团队联合上海市疾病预防控制中心、昆山杜克大学疫苗交付研究创新实验室(VaxL...

2012—2022年上海孕期流感疫苗接种的人口学特征及与早产结局关联研究
本文由复旦大学蒋泓教授团队与上海市疾病预防控制中心联合发表于《临床儿科杂志》。研究基于2012—20...





